Fen Bilimleri – 8. Sınıf – Ünite4: Madde ve Endüstri – Bölüm 5: Maddenin Isıyla Etkileşimi
Isı:
Sıcaklıkları farklı iki madde arasında gerçekleşen enerji aktarımına ısı denir.
Isının birimi Kalori veya Joule’dür
Kalorimetre kabıyla ölçülür.
Öz Isı:
Bir maddenin 1 gramının sıcaklığını
1 °C arttırmak için gereken enerjiye denir.

Her maddenin ayrı bir öz ısı değeri vardır. Bunun için öz ısı maddenin ayırt edici özelliğidir.
Öz ısının birimi J/g °C veya Cal/ g °C ‘tur.
c harfiyle gösterilir
Bazı maddelerin öz ısı değerleri ( J/g °C):
Su : 4.18
Alkol: 2.54
Zeytinyağı: 1.96
Demir: 0.36
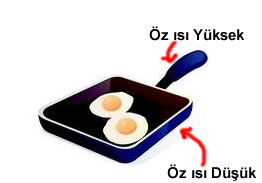
Öz Isısı Çok Olan;
– Geç Isınır
– Geç Soğur
– İyi ısı iletkeni değildir.
Öz Isısı Az Olan;
– Çabuk ısınır
– Çabuk soğur
– İyi ısı iletkenidir.
Eşit süre ısıtılan aynı sıcaklıktaki farklı türden sıvılarda sıcaklık değişimi aynı olmaz
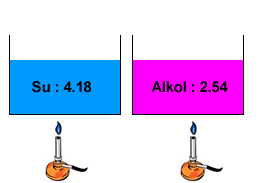
Suyun öz ısısı alkolden fazla olduğu için eşit süre sonunda alkolün sıcaklığı daha fazla olur.
Kütlenin Sıcaklık Değişimine Etkisi
Eşit şartlar altında kütlesi fazla olan sıvı daha geç ısınır.
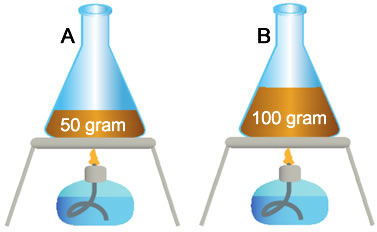
Eşit süre sonunda B kabındaki sıvının sıcaklığı daha azdır.
Isı Alışverişi ve Hal Değişimi
Bir maddenin hal değiştirmesini ısı alışverişi sağlar.
ERİME – BUHARLAŞMA : Madde ısı alır
DONMA – YOĞUŞMA : Madde ısı verir
Hal Değişimi Isıları
Le: Erime ısısı
Ld: Donma Isısı
Lb: Buharlaşma ısısı
Ly: Yoğuşma ısısı
Hal değiştirme ısılarının birimi g/J veya g/cal’dir.
Hal değiştirme ısısı maddenin ayırt edici özelliğidir.
Bir maddenin bir gramının bir halden diğer hale geçmesi için gerekli ısı miktarıdır.
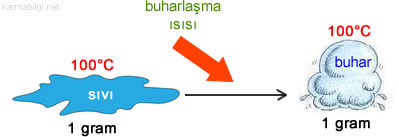
Örneğin: 1 gram kaynama sıcaklığındaki sıvı suyun yine aynı sıcaklıkta gaz hale geçmesi için gerekli olan ısıya buharlaşma ısısı denir.
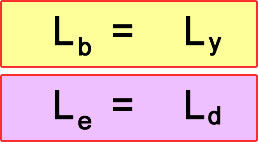
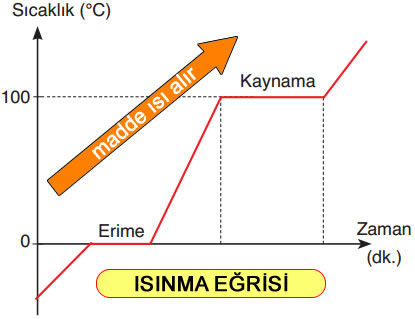
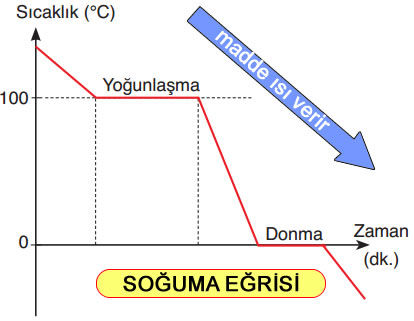
Sıcaklık Zaman Grafikleri
Saf maddelerin erime noktası, donma noktası, kaynama noktası ve yoğuşma noktası belirli değerlerdir.
Örneğin su 0 °C ‘ta donar. Yine aynı sıcaklıkta erir.
Madde hal değiştirirken maddenin tamamı hal değiştirinceye kadar sıcaklık sabit kalır.
Sıcaklık zaman grafiğine bakarak maddenin hangi aralıklarda hal değiştirdiğini görebiliriz.