Fen Bilimleri – 7. Sınıf – Ünite 4: Saf Madde ve Karışımlar – Bölüm 3
Doğadaki çoğu madde karışım özelliğindedir.
Örnek verecek olursak yiyeceklerin neredeyse tamamı, hava, çeşme suyu, denizler, toprak, tahta, ağaçlar vb. birer karışımdır.
Gördüğümüz gibi doğadaki maddelerin büyük çoğunluğu karışım halinde bulunur.
Karışım Nedir?
İki veya daha fazla madde aralarında kimyasal bağ olmadan bir araya gelirse bu karışım olur.
Örneğin tuz ve şekeri bir kaba koyarsak aralarında kimyasal bağ gerçekleşmez. Tuz hala tuz, şeker hala şekerdir. Sadece iç içe geçmiş durumdadırlar.
Soluduğumuz hava da bir karışımdır.
Havada Azot, Oksijen, karbondioksit gibi gazlar bulunur.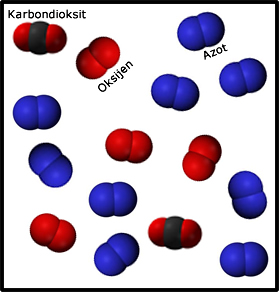
Yukarıda hava karışımının içinde bulunan tanecikler görülmekte. Hava çeşitli bileşik ve elementlerden oluşmuş bir karışımdır.
Şekilden de görebileceğimiz gibi karışımı oluşturan tanecikler birbirinden ayrıdır, yani aralarında bağ yoktur.
Karışımların Özellikleri
- Karışımı oluşturan maddeler kimyasal özelliklerini kaybetmez.
- Karışımlarda fiziksel değişim gerçekleşir.
- Karışımların belirli bir erime-kaynama noktası yoktur.
- Karışımların belirli bir birleşme oranı yoktur.
- Karışımlar formül veya sembolle gösterilmez.
- Karışımı oluşturan maddeler fiziksel yollarla ayrılabilirler. Bu yöntemler buharlaştırma, süzme, eleme, suda yüzdürme, mıknatısla çekme, ayrımsal damıtma, ayırma hunisi vb.
KARIŞIM TÜRLERİ
Heterojen Karışım – Adi Karışım
Karışımı oluşturan maddeler karışımın her yerinde eşit olarak dağılmıyorsa bu tür karışımlara heterojen karışım denir.
Heterojen karışım her yerinde aynı özelliği göstermez.
Örneğin kum ve su karışımını düşünelim.
Kum dibe çöker su ise üstte kalır. İki madde tam olarak birbiri içinde dağılmaz. Karşımın üstünde su altında ise kum vardır.
Heterojen Karışıma Örnekler
Toprak, Tebeşir tozu+su, sıvı yağ+su, tuz+şeker, çorba, yemekler, odun talaşı su karışımı vb.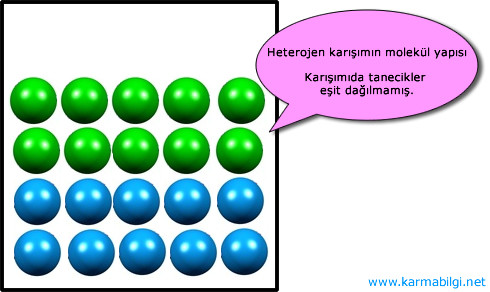
Homojen Karışım – Çözelti
Karışımı oluşturan maddeler karışımın her yerinde eşit olarak dağılmışsa bu bir homojen karışımdır.
Homojen karışım her yerinde aynı özelliği gösterir.
Örneğin çeşme suyu, su ve minerallerden oluşan bir karışımdır. Bir bardak suyu düşünelim. Bardağın üstü, altı, sağı solu, yani, her yerinde aynı özellikte su bulunur. Demek ki çeşme suyu homojen bir karışımdır.
Homojen Karımıma Örnekler
Tuzlu su(karıştırılmış), şekerli su, kola, gazoz, hava, metal alaşımları (çelik, pirinç, lehim), kolonya, sirke, tentürdiyot, çeşme suyu.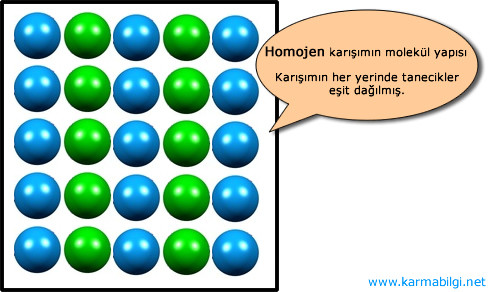
Aşağıda homojen ve heterojen karışım resimleri gösterilmiştir.
Homojen karışımlarda yani çözeltilerde karışımın çok iyi gerçekleşmesinin nedeni karışımı oluşturan maddelerden birinin diğerinin çözmesidir.
Örnek verirsen tuzlu suyu düşünelim.
Su, tuzu içinde çözer. Yani homojen şekilde karıştırır.
Çözücü ve çözünen örnekleri:
Tuzlu su ———— Çözücü : Su, Çözünen : Tuz
Mürekkepli su —– Çözücü : Su, Çözünen : Mürekkep
Çay —————– Çözücü : Su, Çözünen : Çay
Çeşme suyu ——- Çözücü : Su, Çözünen : Mineraller
Çözücü ve çözüneni bulurken zorlanırsak şu önemli noktaları hatırlamalıyız:
- Sulu çözeltilerde su her zaman çözücüdür.
- Su olmayan çözeltilerde karışımda hangi maddenin oranı daha fazlaysa çözücü o maddedir.
Çözeltiler 3 dala ayrılır.
1. Elektriği iletme özelliğine göre çözeltiler
A- ELEKTROLİT ÇÖZELTİ
Elektrik akımını iletebilen çözeltilerdir.
Limonlu su, tuzlu su, sirkeli su elektrolittir.
Elektrolit çözeltilerde çözünen madde +, – yüklü iyonlara ayrışarak çözünür. İletkenliğin nedeni budur.
B- ELEKTROLİT OLMAYAN ÇÖZELTİ
Elektrik akımını iletmeyen karışımlardır.
Şekerli su, alkollü su, hava elektrolit değildir.
Elektrolit olmayan çözeltilerde çözünen madde yüksüz moleküllere ayrılarak karışır. Bu nedenle elektriği iletmez.
2. Çözünen Madde Miktarına Göre Karışımlar
A- DERİŞİK ÇÖZELTİ
İçinde çözünen madde daha çok olan çözeltidir. Örneğin aynı miktarda iki bardak çaydan içine daha fazla şeker koyulan diğerinden daha derişiktir.
B- SEYRELTİK ÇÖZELTİ
Seyreltik Çözelti içinde çözünen miktarı az olan karışımdır.
Aynı miktardaki iki bardak çaydan içine daha az şeker atılan seyreltiktir.
Derişik ve seyreltik çözeltileri daha ayrıntılı incelemek için tıklayın >>>
3. Fiziksel Hale Göre Çözeltiler
Çözeltileri oluşturun karışımlar katı-sıvı-gaz olabilir.
Örneğin şekerli su çözeltisi bir katı-sıvı çözeltisidir. Şeker katı, su ise sıvıdır
